Kirjoittaja:
Mark Sanchez
Luomispäivä:
3 Tammikuu 2021
Päivityspäivä:
1 Heinäkuu 2024

Sisältö
- Askeleet
- Menetelmä 1/2: Massaprosentin määrittäminen määritettyjen painojen perusteella
- Menetelmä 2/2: Massaprosentin määrittäminen, kun massaa ei ole määritetty
Massaprosentti määrittää alkuaineiden prosenttiosuuden kemiallisessa yhdisteessä. Massaprosentin löytämiseksi sinun on tiedettävä yhdisteen sisältämien alkuaineiden moolimassa (grammoina moolia kohti) tai kunkin komponentin grammamäärä tietyn liuoksen saamiseksi.Massaprosentti lasketaan yksinkertaisesti: riittää, kun jaetaan alkuaineen (tai komponentin) massa koko yhdisteen (tai liuoksen) massalla.
Askeleet
Menetelmä 1/2: Massaprosentin määrittäminen määritettyjen painojen perusteella
 1 Valitse yhtälö kemiallisen yhdisteen painoprosentin määrittämiseksi. Massaprosentti lasketaan seuraavalla kaavalla: massaprosentti = (komponentin massa / yhdisteen kokonaismassa) x 100. Prosentin saamiseksi jakamisen tulos kerrotaan 100: lla.
1 Valitse yhtälö kemiallisen yhdisteen painoprosentin määrittämiseksi. Massaprosentti lasketaan seuraavalla kaavalla: massaprosentti = (komponentin massa / yhdisteen kokonaismassa) x 100. Prosentin saamiseksi jakamisen tulos kerrotaan 100: lla. - Kirjoita ongelman ratkaisun alkuun tasa -arvo: massaprosentti = (komponentin massa / yhdisteen kokonaismassa) x 100.
- Kiinnostavan komponentin massan pitäisi olla ongelman tilassa. Jos massaa ei ole annettu, siirry seuraavaan osaan, jossa selitetään, kuinka massaprosentti määritetään tuntemattomalla massalla.
- Kemiallisen yhdisteen kokonaismassa määritetään lisäämällä kaikkien tämän yhdisteen (tai liuoksen) osana olevien alkuaineiden (komponenttien) massat.
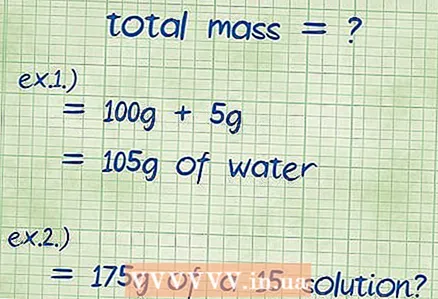 2 Laske yhdisteen kokonaismassa. Jos tiedät kaikkien yhdisteen muodostavien komponenttien massat, lisää ne vain yhteen, ja tällä tavalla löydät tuloksena olevan yhdisteen tai liuoksen kokonaismassan. Käytät tätä massaa massaprosenttien yhtälön nimittäjänä.
2 Laske yhdisteen kokonaismassa. Jos tiedät kaikkien yhdisteen muodostavien komponenttien massat, lisää ne vain yhteen, ja tällä tavalla löydät tuloksena olevan yhdisteen tai liuoksen kokonaismassan. Käytät tätä massaa massaprosenttien yhtälön nimittäjänä. - Esimerkki 1: Mikä on 5 gramman natriumhydroksidin massaprosentti liuotettuna 100 grammaan vettä?
- Liuoksen kokonaismassa on yhtä suuri kuin natriumhydroksidin ja veden määrä: 100 g + 5 g antaa 105 g.
- Esimerkki 2: Kuinka paljon natriumkloridia ja vettä tarvitset 175 gramman 15 -prosenttisen liuoksen valmistamiseen?
- Tässä esimerkissä annetaan kokonaismassa ja vaadittu prosenttiosuus, ja on löydettävä liuokseen lisättävän aineen määrä. Kokonaispaino on 175 grammaa.
- Esimerkki 1: Mikä on 5 gramman natriumhydroksidin massaprosentti liuotettuna 100 grammaan vettä?
 3 Määritä määritetyn komponentin massa. Jos sinua pyydetään laskemaan "massaprosentti", sinun pitäisi selvittää, kuinka monta prosenttia aineen kokonaismassasta on tietyn komponentin massa. Kirjaa määritetyn komponentin massa. Tämä on massaprosentin kaavan osoittaja.
3 Määritä määritetyn komponentin massa. Jos sinua pyydetään laskemaan "massaprosentti", sinun pitäisi selvittää, kuinka monta prosenttia aineen kokonaismassasta on tietyn komponentin massa. Kirjaa määritetyn komponentin massa. Tämä on massaprosentin kaavan osoittaja. - Esimerkki 1: Tietyn komponentin - natriumhydrokloridin - massa on 5 grammaa.
- Esimerkki 2: Tässä esimerkissä annetun komponentin massa on tuntematon ja se on löydettävä.
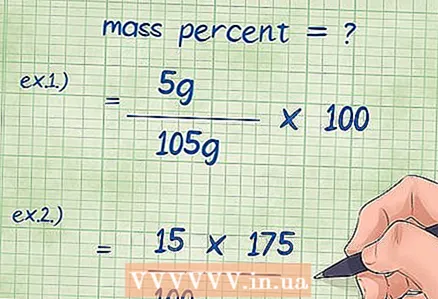 4 Liitä arvot massaprosenttiyhtälöön. Kun olet määrittänyt kaikki vaaditut arvot, liitä ne kaavaan.
4 Liitä arvot massaprosenttiyhtälöön. Kun olet määrittänyt kaikki vaaditut arvot, liitä ne kaavaan. - Esimerkki 1: massaprosentti = (komponentin massa / yhdisteen kokonaismassa) x 100 = (5 g / 105 g) x 100.
- Esimerkki 2: massaprosentin kaava on muutettava siten, että kemiallisen komponentin tuntematon massa voidaan löytää: komponentin massa = (massaprosentti * yhdisteen kokonaismassa) / 100 = (15 * 175) / 100.
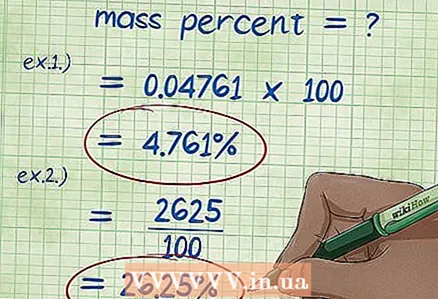 5 Laske massaprosentti. Kun olet korvannut kaikki massaprosentin arvot kaavassa, suorita tarvittavat laskelmat. Jaa komponentin massa kemiallisen yhdisteen tai liuoksen kokonaispainolla ja kerro 100: lla. Tuloksena on kyseisen komponentin massaprosentti.
5 Laske massaprosentti. Kun olet korvannut kaikki massaprosentin arvot kaavassa, suorita tarvittavat laskelmat. Jaa komponentin massa kemiallisen yhdisteen tai liuoksen kokonaispainolla ja kerro 100: lla. Tuloksena on kyseisen komponentin massaprosentti. - Esimerkki 1: (5/105) x 100 = 0,04761 x 100 = 4,761%. Siten 5 gramman natriumhydrokloridin painoprosentti liuotettuna 100 grammaan vettä on 4,761%.
- Esimerkki 2: Uudelleen kirjoitettu lauseke komponentin massaprosentille on (massaprosentti * aineen kokonaismassa) / 100, josta löydämme: (15 * 175) / 100 = (2625) / 100 = 26,25 grammaa natriumkloridia.
- Tarvittava vesimäärä löydetään vähentämällä komponentin massa liuoksen kokonaismassasta: 175 - 26,25 = 148,75 grammaa vettä.
Menetelmä 2/2: Massaprosentin määrittäminen, kun massaa ei ole määritetty
 1 Valitse kaava kemiallisen yhdisteen painoprosentille. Perusyhtälö massaprosentin löytämiseksi on seuraava: massaprosentti = (alkuaineen moolimassa / yhdisteen kokonaismolekyylipaino) x 100. Aineen moolimassa on tietyn aineen yhden moolin massa, kun taas molekyylimassa on yhden moolin massa kaikista kemikaaleista. Jakauma kerrotaan 100: lla, jotta saadaan prosentit.
1 Valitse kaava kemiallisen yhdisteen painoprosentille. Perusyhtälö massaprosentin löytämiseksi on seuraava: massaprosentti = (alkuaineen moolimassa / yhdisteen kokonaismolekyylipaino) x 100. Aineen moolimassa on tietyn aineen yhden moolin massa, kun taas molekyylimassa on yhden moolin massa kaikista kemikaaleista. Jakauma kerrotaan 100: lla, jotta saadaan prosentit. - Kirjoita ongelman ratkaisun alkuun tasa -arvo: massaprosentti = (alkuaineen moolimassa / yhdisteen moolimassa) x 100.
- Molemmat määrät mitataan grammoina moolia kohti (g / mol).
- Jos sinulle ei anneta massoja, tietyn aineen alkuaineen massaprosentti voidaan löytää käyttämällä moolimassaa.
- Esimerkki 1: Etsi vedyn massaprosentti vesimolekyylistä.
- Esimerkki 2: Etsi hiiliprosentti glukoosimolekyylistä.
 2 Kirjoita ylös kemiallinen kaava. Jos esimerkki ei anna määritettyjen aineiden kemiallisia kaavoja, kirjoita ne itse. Jos tehtävä sisältää tarvittavat kaavat kemiallisille aineille, voit ohittaa tämän vaiheen ja siirtyä suoraan seuraavaan vaiheeseen (etsi jokaisen elementin massa).
2 Kirjoita ylös kemiallinen kaava. Jos esimerkki ei anna määritettyjen aineiden kemiallisia kaavoja, kirjoita ne itse. Jos tehtävä sisältää tarvittavat kaavat kemiallisille aineille, voit ohittaa tämän vaiheen ja siirtyä suoraan seuraavaan vaiheeseen (etsi jokaisen elementin massa). - Esimerkki 1: Kirjoita muistiin veden kemiallinen kaava, H2O.
- Esimerkki 2: Kirjoita ylös glukoosin kemiallinen kaava, C6H12O6.
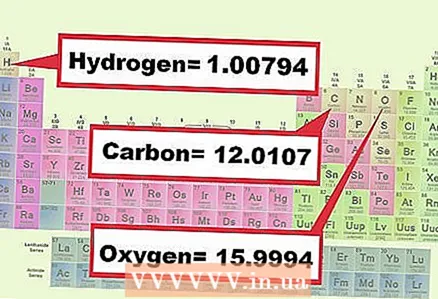 3 Etsi kunkin elementin massa yhdisteestä. Määritä kunkin alkuaineen moolipaino kemiallisessa kaavassa jaksollisen taulukon mukaisesti. Tyypillisesti elementin massa ilmoitetaan sen kemiallisen symbolin alla. Kirjoita muistiin kaikkien yhdisteiden muodostavien alkuaineiden moolimassat.
3 Etsi kunkin elementin massa yhdisteestä. Määritä kunkin alkuaineen moolipaino kemiallisessa kaavassa jaksollisen taulukon mukaisesti. Tyypillisesti elementin massa ilmoitetaan sen kemiallisen symbolin alla. Kirjoita muistiin kaikkien yhdisteiden muodostavien alkuaineiden moolimassat. - Esimerkki 1: Etsi hapen (15.9994) ja vedyn (1.0079) moolimassat.
- Esimerkki 2: Etsi hiilen (12,0107), hapen (15,9994) ja vedyn (1,0079) moolimassat.
 4 Kerro kunkin elementin moolimassa sen moolijakeella. Määritä, kuinka monta moolia kustakin alkuaineesta sisältää tietty kemikaali, eli alkuaineiden mooliosuudet. Moolijakeet annetaan kaavan elementtisymbolien alareunassa olevilla numeroilla. Kerro kunkin elementin moolimassa sen moolijakeella.
4 Kerro kunkin elementin moolimassa sen moolijakeella. Määritä, kuinka monta moolia kustakin alkuaineesta sisältää tietty kemikaali, eli alkuaineiden mooliosuudet. Moolijakeet annetaan kaavan elementtisymbolien alareunassa olevilla numeroilla. Kerro kunkin elementin moolimassa sen moolijakeella. - Esimerkki 1: vetymerkin alla on 2 ja happisymbolin alla (vastaa numeron puuttumista). Siten vedyn moolimassa tulisi kertoa 2: 1,00794 X 2 = 2,01588; jätämme hapen moolimassan ennalleen, 15,9994 (eli kerrotaan 1: llä).
- Esimerkki 2: hiilisymbolin alla on 6, vedyn 12 ja hapen 6. Kun kerrotaan alkuaineiden moolimassat näillä numeroilla, löydämme:
- hiili: (12,0107 * 6) = 72,0642
- vety: (1,00794 * 12) = 12,09528
- happi: (15,9994 * 6) = 95,9964
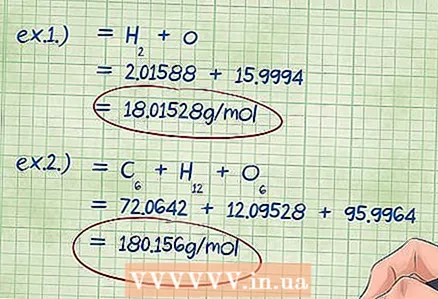 5 Laske yhdisteen kokonaismassa. Laske yhteen kaikkien tämän yhdisteen sisältämien alkuaineiden löydetyt massat. Elementtien moolimassojen summa kerrottuna moolijakeilla antaa sinulle kemiallisen yhdisteen kokonaismassan. Tämä luku on massaprosentin kaavan jakaja.
5 Laske yhdisteen kokonaismassa. Laske yhteen kaikkien tämän yhdisteen sisältämien alkuaineiden löydetyt massat. Elementtien moolimassojen summa kerrottuna moolijakeilla antaa sinulle kemiallisen yhdisteen kokonaismassan. Tämä luku on massaprosentin kaavan jakaja. - Esimerkki 1: Lisää 2,01588 g / mol (kahden moolin vetyatomien massa) 15,9994 g / mol (yhden moolin happiatomien massa), tulos on 18,01528 g / mol.
- Esimerkki 2: Lisää löydetyt moolimassat: hiili + vety + happi = 72,0642 + 12,09528 + 95,9964 = 180,156 g / mol.
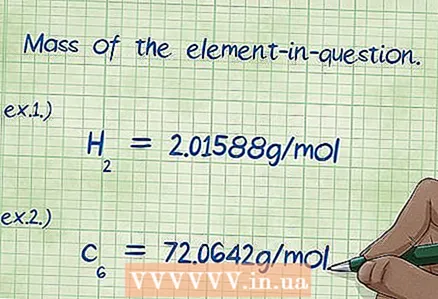 6 Määritä kiinnostavan elementin massa. Jos sinua pyydetään löytämään "massaprosentti", sinun on laskettava tietyn elementin massa, joka on osa yhdistettä, prosentteina kaikkien alkuaineiden kokonaismassasta. Etsi tietyn elementin massa ja kirjoita se muistiin. Tätä varten on tarpeen kertoa alkuaineen moolimassa sen moolijakeella. Tämän seurauksena saat massaprosentin kaavan osoittimen arvon.
6 Määritä kiinnostavan elementin massa. Jos sinua pyydetään löytämään "massaprosentti", sinun on laskettava tietyn elementin massa, joka on osa yhdistettä, prosentteina kaikkien alkuaineiden kokonaismassasta. Etsi tietyn elementin massa ja kirjoita se muistiin. Tätä varten on tarpeen kertoa alkuaineen moolimassa sen moolijakeella. Tämän seurauksena saat massaprosentin kaavan osoittimen arvon. - Esimerkki 1: Yhdisteen vedyn massa on 2,01588 g / mol (kahden moolin vetyatomien massa).
- Esimerkki 2: Hiilen massa yhdisteessä on 72,0642 g / mol (kuuden moolin hiiliatomien massa).
 7 Korvaa numeeriset arvot massaprosenttiyhtälöllä. Kun olet määrittänyt kaikkien määrien arvot, liitä ne ensimmäisessä vaiheessa annettuun kaavaan: massaprosentti = (alkuaineen moolimassa / yhdisteen kokonaismolekyylipaino) x 100.
7 Korvaa numeeriset arvot massaprosenttiyhtälöllä. Kun olet määrittänyt kaikkien määrien arvot, liitä ne ensimmäisessä vaiheessa annettuun kaavaan: massaprosentti = (alkuaineen moolimassa / yhdisteen kokonaismolekyylipaino) x 100. - Esimerkki 1: massaprosentti = (alkuaineen moolimassa / yhdisteen kokonaismolekyylimassa) x 100 = (2,01588 / 18,01528) x 100.
- Esimerkki 2: massaprosentti = (alkuaineen moolimassa / yhdisteen moolimassa) x 100 = (72,0642 / 180,156) x 100.
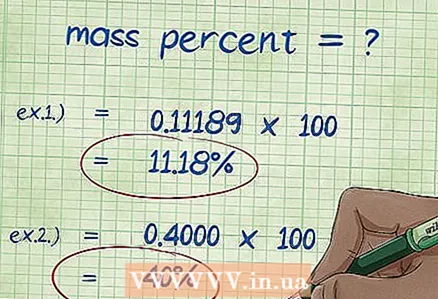 8 Laske massaprosentti. Kun olet korvannut numeeriset arvot, suorita vaaditut aritmeettiset toiminnot.Jaa alkuaineen massa yhdisteen kokonaismassalla ja kerro 100: lla. Tuloksena on alkuaineen massaprosentti.
8 Laske massaprosentti. Kun olet korvannut numeeriset arvot, suorita vaaditut aritmeettiset toiminnot.Jaa alkuaineen massa yhdisteen kokonaismassalla ja kerro 100: lla. Tuloksena on alkuaineen massaprosentti. - Esimerkki 1: massaprosentti = (alkuaineen moolimassa / yhdisteen kokonaismolekyylimassa) x 100 = (2,01588 / 18,01528) x 100 = 0,111189 x 100 = 11,18%. Siten vetyatomien massaprosentti vesimolekyylissä on 11,18%.
- Esimerkki 2: massaprosentti = (alkuaineen moolimassa / yhdisteen kokonaismolekyylimassa) x 100 = (72,0642 / 180,156) x 100 = 0,4000 x 100 = 40,00%. Siten hiiliatomien painoprosentti glukoosimolekyylissä on 40,00%.



