Kirjoittaja:
Frank Hunt
Luomispäivä:
13 Maaliskuu 2021
Päivityspäivä:
1 Heinäkuu 2024

Sisältö
- Astua
- Menetelmä 1/3: pH-mittarin käyttö
- Menetelmä 2/3: Lakmuspaperilla
- Menetelmä 3/3: pH: n ymmärtäminen
On tärkeää mitata veden pH - happamuusaste tai emäksisyys. Vedet käyttävät kasvit ja eläimet, joista olemme riippuvaisia, ja juomme sitä joka päivä. Veden pH-arvo voi olla osoitus mahdollisesta kontaminaatiosta, joten veden pH-arvon mittaaminen voi olla tärkeä kansanterveysalan varotoimenpide.
Astua
Menetelmä 1/3: pH-mittarin käyttö
 Kalibroi mittapää ja mittari tehtaan ohjeiden mukaisesti. Saatat joutua kalibroimaan mittarin käyttämällä ainetta, jonka pH-arvo tunnetaan. Mittaria voidaan säätää kyseisen aineen mukaan. Jos aiot testata vettä laboratorion ulkopuolella, on suositeltavaa suorittaa tämä kalibrointi muutama tunti ennen kenttätestausta.
Kalibroi mittapää ja mittari tehtaan ohjeiden mukaisesti. Saatat joutua kalibroimaan mittarin käyttämällä ainetta, jonka pH-arvo tunnetaan. Mittaria voidaan säätää kyseisen aineen mukaan. Jos aiot testata vettä laboratorion ulkopuolella, on suositeltavaa suorittaa tämä kalibrointi muutama tunti ennen kenttätestausta. - Huuhtele mittapää puhtaalla vedellä ennen käyttöä. Kuivaa puhtaalla liinalla.
 Ota vesinäyte ja kaada se puhtaaseen astiaan.
Ota vesinäyte ja kaada se puhtaaseen astiaan.- Veden on oltava riittävän syvä upottamaan elektrodin kärki.
- Jätä näytettä hetkeksi lämpötilan vakiintumiseksi.
- Mittaa näytteen lämpötila lämpömittarilla.
 Säädä mittari näytteen lämpötilalla. Veden lämpötila vaikuttaa anturin herkkyyteen, joten mittaus voi olla tarkka vain antamalla lämpötilatiedot.
Säädä mittari näytteen lämpötilalla. Veden lämpötila vaikuttaa anturin herkkyyteen, joten mittaus voi olla tarkka vain antamalla lämpötilatiedot.  Aseta koetin näytteeseen. Odota, että mittari saavuttaa tasapainon. Mittari on vakaassa tilassa, kun lukema on vakaa.
Aseta koetin näytteeseen. Odota, että mittari saavuttaa tasapainon. Mittari on vakaassa tilassa, kun lukema on vakaa.  Lue näytteen pH-mittaus. PH-mittari antaa tuloksen asteikolla 0-14. Jos vesi on puhdasta, arvo on noin 7. Kirjoita havainnot.
Lue näytteen pH-mittaus. PH-mittari antaa tuloksen asteikolla 0-14. Jos vesi on puhdasta, arvo on noin 7. Kirjoita havainnot.
Menetelmä 2/3: Lakmuspaperilla
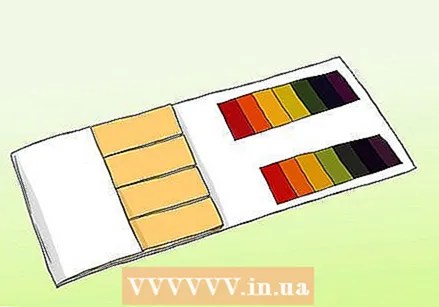 Opi ero pH-paperin ja lakmuspaperin välillä. Voit käyttää pH-paperia saadaksesi näytteen tarkan lukeman. PH-paperia ei kuitenkaan pidä sekoittaa tavalliseen lakmuspaperiin. Molempia voidaan käyttää happojen ja emästen testaamiseen, mutta ne eroavat toisistaan tärkeiltä osin.
Opi ero pH-paperin ja lakmuspaperin välillä. Voit käyttää pH-paperia saadaksesi näytteen tarkan lukeman. PH-paperia ei kuitenkaan pidä sekoittaa tavalliseen lakmuspaperiin. Molempia voidaan käyttää happojen ja emästen testaamiseen, mutta ne eroavat toisistaan tärkeiltä osin. - pH-nauhat sisältävät sarjan indikaattoripalkkeja, jotka muuttavat väriä liuokselle altistettaessa. Happojen ja emästen vahvuus kussakin tankossa on erilainen. Muutoksen jälkeen värikuviota voidaan verrata sarjan mukana toimitettuihin näytteisiin.
- Lakmuspaperi on paperiliuska, joka sisältää happoa tai emästä (emäksistä). Yleisimmät raidat ovat punaiset (hapoilla, jotka reagoivat emästen kanssa) ja siniset (emästen kanssa, jotka reagoivat happojen kanssa). Punaiset raidat muuttuvat sinisiksi, jos aine on emäksistä, ja siniset raidat muuttuvat punaisiksi, jos aine on hapan. Lakmuspapereita voidaan käyttää nopeasti ja helposti testinä, mutta halvimmat lajikkeet eivät aina anna tarkkaa mittausta ratkaisun vahvuudesta.
 Ota näyte vedestä ja kaada se puhtaaseen astiaan. Veden on oltava riittävän syvä upottamaan nauha.
Ota näyte vedestä ja kaada se puhtaaseen astiaan. Veden on oltava riittävän syvä upottamaan nauha.  Kasta testiliuska näytteeseen. Muutaman sekunnin valotus riittää. Paperin osoitinpalkit muuttavat väriä hetken kuluttua.
Kasta testiliuska näytteeseen. Muutaman sekunnin valotus riittää. Paperin osoitinpalkit muuttavat väriä hetken kuluttua.  Vertaa testiliuskan päätä paperin mukana toimitettuun värikarttaan. Kortin värin tai värien on vastattava testiliuskan väriä tai värejä. Värikartta yhdistää sitten värikuviot pH-tasoihin.
Vertaa testiliuskan päätä paperin mukana toimitettuun värikarttaan. Kortin värin tai värien on vastattava testiliuskan väriä tai värejä. Värikartta yhdistää sitten värikuviot pH-tasoihin.
Menetelmä 3/3: pH: n ymmärtäminen
 Opi kuinka hapot ja emäkset määritellään. Happamuus ja emäksisyys (termi, jota käytetään kuvaamaan emäksiä) määritetään molemmat vetyionien avulla, joita ne luovuttavat tai ottavat. Happo on aine, joka luovuttaa (tai "lahjoittaa") vetyioneja, ja emäs on aine, joka absorboi ylimääräisiä vetyioneja.
Opi kuinka hapot ja emäkset määritellään. Happamuus ja emäksisyys (termi, jota käytetään kuvaamaan emäksiä) määritetään molemmat vetyionien avulla, joita ne luovuttavat tai ottavat. Happo on aine, joka luovuttaa (tai "lahjoittaa") vetyioneja, ja emäs on aine, joka absorboi ylimääräisiä vetyioneja.  Ymmärrä pH-asteikko. PH-lukua käytetään vesiliukoisten aineiden happamuuden tai emäksisyyden mittaamiseen. Vedessä on normaalisti sama määrä hydroksidi-ioneja (OH−) ja hydrroniumioneja (H3O +). Hydroksidi- ja hydrroniumionien suhde muuttuu, kun veteen lisätään happamia tai emäksisiä aineita.
Ymmärrä pH-asteikko. PH-lukua käytetään vesiliukoisten aineiden happamuuden tai emäksisyyden mittaamiseen. Vedessä on normaalisti sama määrä hydroksidi-ioneja (OH−) ja hydrroniumioneja (H3O +). Hydroksidi- ja hydrroniumionien suhde muuttuu, kun veteen lisätään happamia tai emäksisiä aineita. - Sitä pidetään yleensä asteikolla, joka vaihtelee 0: sta 14: een (vaikka aineet saattavatkin jäädä tämän alueen ulkopuolelle). Neutraalien aineiden pisteet ovat noin 7, happamien aineiden alle 7 ja emäksisten aineiden yli 7.
- PH-asteikko on logaritminen, mikä tarkoittaa, että kokonaislukuerot edustavat kymmenen kertaa happamuutta tai emäksisyyttä. Esimerkiksi aine, jonka pH on 2, on kymmenen kertaa happamampi kuin aine, jonka pH on 3, ja 100 kertaa happamampi kuin aine, jonka pH on 4. Vaaka toimii samalla tavalla alkalisten aineiden kanssa, minkä tahansa kokonaisluku edustaa kymmenkertaista eroa.
 Opi miksi testaamme veden pH: n. Puhtaan veden pH on 7, mutta hollantilaisen vesijohtoveden pH on yleensä 7,5–8,3. Erittäin hapan vesi (vesi, jolla on alhainen pH-arvo) liuottaa todennäköisemmin myrkyllisiä kemikaaleja. Nämä voivat saastuttaa vettä ja tehdä siitä vaarallista juoda.
Opi miksi testaamme veden pH: n. Puhtaan veden pH on 7, mutta hollantilaisen vesijohtoveden pH on yleensä 7,5–8,3. Erittäin hapan vesi (vesi, jolla on alhainen pH-arvo) liuottaa todennäköisemmin myrkyllisiä kemikaaleja. Nämä voivat saastuttaa vettä ja tehdä siitä vaarallista juoda. - Yleensä on suositeltavaa testata pH paikan päällä. Jos otat vesinäytteen laboratoriotutkimusta varten, ilmasta peräisin oleva hiilidioksidi (CO2) voi liueta veteen. Liuennut hiilidioksidi reagoi vedessä olevien ionien kanssa ja lisää happamuutta emäksisissä tai neutraaleissa liuoksissa. Hiilidioksidikontaminaation välttämiseksi vesi on testattava kahden tunnin kuluessa keräyksestä.